
Astrocitos, las Estrellas Ignoradas
Artículo y traducción de Elena Blanco-Suárez
Normalmente se usa el término “célula cerebral” para referirse a las neuronas, como si fueran el único tipo celular que hay en el cerebro. Nada más lejos de la realidad. Las neuronas pueden considerarse como la unidad celular más importante de nuestro sistema nervioso, ya que son las células que transmiten información a través de señales eléctricas y químicas. No discutiré que las neuronas son tremendamente importantes, pero si tengo que pelearme por ignorar a las otras “células cerebrales” que componen nuestro cerebro, lo hago.
De hecho, la mitad del contenido celular de nuestro cerebro es realmente “glía”. Este término incluye oligodendrocitos, microglia y astrocitos, tres tipos de células no-neuronales que están en el cerebro junto a otras células que componen los vasos sanguíneos que lo recorren. “Glía” es una palabra derivada del griego que significa “pegamento”, ya que inicialmente se creía que no eran más que un grupo de células no-neuronales que estaban en el cerebro con la única función de mantener todo junto, todo “pegado”.
Sin embargo, las células gliales son bastante diversas, y tienen más que una mera función estructural.
Los astrocitos son las células gliales más abundantes. Su nombre, también del griego, significa “célula estrellada”. Entre sus varias funciones encontramos la provisión de nutrientes y apoyo físico a las neuronas, así como el mantenimiento del delicado equilibrio químico cerebral. Los astrocitos han recibido bastante atención debido a que son los encargados de formar la cicatriz glial. Al igual que nuestra piel, nuestro cerebro también cicatriza.
ASTROCITOS: ALGO MAS QUE PEGAMENTO

Astrocitos (verde) y neuronas (rojo) fotografiados en la corteza visual de ratón. En azul, los núcleos celulares. Fotografía: Elena Blanco-Suárez.
En los últimos años, científicos se han dado cuenta de que los astrocitos en realidad hacen algo más que simplemente mantener todo en su sitio y crear cicatrices. De hecho, vieron que los astrocitos tienen un rol muy activo a la hora de ayudar a las neuronas a crear y desarrollar sus conexiones, llamadas sinapsis.
Los astrocitos producen y secretan proteínas que envían a las neuronas, como instrucciones. El Dr. Ben Barres fue un pionero investigando el rol de estas proteínas, o factores si lo prefieres.
Por ejemplo, thrombospondins y hevin son algunos de estos factores que los astrocitos producen y secretan para promover la formación estructural de sinapsis. Sin embargo, dichas sinapsis son “silenciosas” debido a la falta de receptores AMPA (AMPARs). La neurona postsináptica (la “receptora”) necesita esos receptores en particular para recibir las señales (neurotransmisores) que llegan de la neurona presináptica (la “emisora”) para así poder llevar a cabo la transmisión del impulso nerviosa de una neurona a otra.
Las sinapsis atraviesan distintas etapas de desarrollo, maduración y estabilización, y no estaba nada claro que los astrocitos estuvieran realmente involucrados en nada más allá que la formación estructural de las sinapsis. Pero ahora sabemos que los astrocitos realmente son capaces de reclutar esos receptores a la superficie de la neurona postsináptica.
Una vez la estructura de la sinapsis esta lista, los receptores AMPA (AMPARs), los principales receptores de la señal nerviosa excitatoria, serán reclutados gracias a los factores secretados por los astrocitos, proteínas tales como el glipicanos 4 y 6. Los glipicanos 4 y 6 solo insertan un tipo específico de AMPAR en la superficie de la neurona, son AMPAR que no tienen la subunidad GluA2. Los AMPARs están hechos de 2+2 subunidades que van de la GluA1 a la GluA4. El tipo de subunidades que componen el AMPAR depende de la edad, o la región cerebral entre otras cosas.
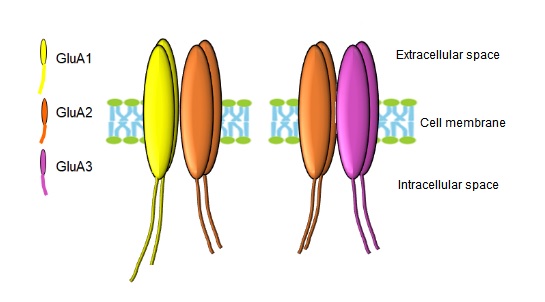
AMPAR son heterotetrameros. Los receptores están compuestos de 4 subunidades, y el tipo de subunidades depende de la edad o de la región cerebral considerada. Por ejemplo, en el hipocampo adulto los AMPARs más comunes están compuestos de 2 unidades GluA2 y 2 GluA1 o 2 GluA3. Imagen: Elena Blanco-Suárez.
En etapas tempranas de desarrollo, los AMPARs normalmente no tienen subunidad GluA2. Esto hace que las sinapsis sean inmaduras y capaces de adaptarse y construir circuitos cerebrales basados en la experiencia a la cual el cerebro está expuesto. Es lo que llamamos plasticidad. Cuanto más envejecemos, más se reduce la plasticidad de nuestro cerebro. Los circuitos cerebrales muestran alta plasticidad en determinados momentos durante el desarrollo, y esos periodos de tiempo es lo que denominamos “periodos críticos”. En parte esta es la razón por la que aprender un idioma parece más difícil cuando somos más mayores, al menos en comparación con los niños que parecen aprender nuevos idiomas sin esfuerzo. Incluso el acento.

Los periodos críticos en humanos. Los sentidos desarrollan sus circuitos en los primeros años de nuestra vida, mientras que la alta plasticidad necesaria para la adquisición del lenguaje ocurre un poco más tarde. El periodo crítico más tardío es el dedicado a la adquisición de procesos cognitivos más altos, como el razonamiento matemático, pensamiento crítico, capacidad de lectura, etc… Imagen adaptada de Jon Bardin. Neurodevelopment: Unlocking the Brain. Nature News Feature, 2012.
Puesto que vimos que los astrocitos están a cargo de la formación estructural de las sinapsis, y de la inserción de los AMPARs en las sinapsis silenciosas para hacerlas funcionales, lo siguiente que nos preguntamos fue: Pueden los astrocitos promover la maduración de las sinapsis.
Según envejecemos, las sinapsis van madurando y esta maduración viene marcada por la sustitución de AMPAR que no contienen la subunidad GluA2, por los que si la contienen. Mi propia investigación ha demostrado que otro factor secretado por astrocitos, llamado Chordin-like 1 (Chrdl1) puede de hecho promover dicha sustitución de los AMPARs, así como la formación de sinapsis nuevas y funcionales.
Esto demuestra que el rol de los astrocitos va más allá de las funciones de mantenimiento que originalmente se les atribuían. Ahora sabemos que también regulan la maduración sináptica.
El trabajo de los astrocitos dura toda la vida
El rol que los astrocitos tienen en maduración nos sugería que también tendrían un papel en la plasticidad cerebral, ya que cuanto más maduras son las neuronas, menor plasticidad muestra el cerebro. Nuestros circuitos necesitan asentarse, ya que no pueden (ni deben) permanecer inmaduros toda la vida. Aunque suene interesante mantener tu cerebro en un estado constante de alta plasticidad, capaz de adaptarse fácilmente, y con alto potencial para aprender lo que sea sin esfuerzo, párate a pensarlo. Querrías que tu cerebro se mantuviese en el mismo estado en el que solía estar cuando eras un niño, en el pico de su plasticidad? No necesariamente, ya que probablemente por tu propio bien es mejor tener circuitos totalmente funcionales y maduros.
Pero existe alguna forma en la que pudiésemos en un preciso instante hacer que el cerebro adulto volviera a su estado de plasticidad de un niño de 5 años? Por ejemplo, a edades más adultas el resultado tras un infarto cerebral no es tan favorable debido a la bajada en plasticidad. Podríamos entonces llamar a los astrocitos para que indujeran plasticidad? Podríamos engañar a nuestro cerebro para que incrementase su plasticidad y reconstruyera los circuitos dañados?
Lo que observe fue que los efectos de los astrocitos en la plasticidad cerebral no estaban restringidos a los periodos críticos, sino que también aparecían patentes en adultos, cuando los circuitos están supuestamente establecidos y menos plásticos. Manipular los factores secretados por astrocitos parece prometedor ya que seriamos capaces de darle un empujón a la habilidad del propio cerebro para repararse a sí mismo en caso de sufrir un infarto cerebral, una lesión traumática cerebral, o cualquier otra enfermedad que dependiera de la plasticidad.
Pero entonces, por qué los astrocitos no vienen al rescate de forma natural?
Esto se debe a que cuando envejecemos, los astrocitos también se ven afectados. De hecho, debido a diferentes cambios, los astrocitos pueden convertirse en enemigos. Por ejemplo, comienzan a eliminar sinapsis que no deberían ser eliminadas, y reducen la producción de colesterol absolutamente necesaria para el cerebro para mantener su buen estado.
Resolver los mecanismos por los cuales los factores secretados por astrocitos pueden formar, desarrollar y madurar sinapsis podría arrojar algo de luz a la cuestión de por qué según pasan los años se van volviendo cada vez más vagos en su importante misión. Saber esto podría ayudar a resolver cómo utilizar el poder de los astrocitos para regular la plasticidad y beneficiar así al cerebro en su madurez.
Referencias
Allen NJ, Bennett ML, Foo LC,Wang GX, Chakraborty C, et al. 2012. Astrocyte glypicans 4 and 6 promote formation of excitatory synapses via GluA1 AMPA receptors. Nature 486:410–14
Bartheld, C. S., Bahney, J. and Herculano‐Houzel, S. 2016, The search for true numbers of neurons and glial cells in the human brain: A review of 150 years of cell counting. J. Comp. Neurol., 524: 3865-3895. doi:10.1002/cne.24040
Blanco-Suarez E, Liu TF, Kopelevich A, Allen NJ. Astrocyte-Secreted Chordin-like 1 Drives Synapse Maturation and Limits Plasticity by Increasing Synaptic GluA2 AMPA Receptors. Neuron. 2018 Dec 5;100(5):1116-1132.e13. doi: 10.1016/j.neuron.2018.09.043. Epub 2018 Oct 18.
Boisvert MM, Erikson GA, Shokhirev MN, Allen NJ. The Aging Astrocyte Transcriptome from Multiple Regions of the Mouse Brain. Cell Rep. 2018 Jan 2;22(1):269-285. doi: 10.1016/j.celrep.2017.12.039.
Christopherson K, Ullian E, Stokes C, Mullowney C, Hell J, et al. 2005. Thrombospondins are astrocyte-secreted proteins that promote CNS synaptogenesis. Cell 120:421–33
Kucukdereli H, Allen NJ, Lee AT, Feng A, Ozlu MI, et al. 2011. Control of excitatory CNS synaptogenesis by astrocyte-secreted proteins Hevin and SPARC. Proc. Natl. Acad. Sci. USA 108:E440–E49

You must be logged in to post a comment.