
Atento a tus Ps y Ts: Cómo las drogas adulteradas revolucionaron la investigación del Parkinson.
Artículo de Drew Schreiner
Traducción de Elena Blanco-Suárez
En 1982, un hombre con una curiosa afección fue ingresado en un hospital de la zona de la Bahía de California. El hombre se encontraba totalmente catatónico (inmóvil), congelado en una postura extraña, como si de una estatua se tratase. Los médicos inicialmente diagnosticaron esquizofrenia catatónica, un sub-tipo de esquizofrenia caracterizada por rigidez y falta de respuesta. Sin embargo, el diagnóstico no encajaba totalmente. El Dr. William Langston examinó al paciente llegando rápidamente a la conclusión de que dicho paciente – George Carrillo – padecía en realidad Parkinson y no esquizofrenia.
Este diagnóstico resultó ser sorprendente. Aunque el Parkinson se caracteriza en parte por alteraciones motoras como temblores y rigidez, también se trata de una enfermedad progresiva, lo que significa que sus síntomas van empeorando lentamente durante el transcurso de los años. Además, estos síntomas normalmente aparecen en torno a los 60 años de edad. El señor Carrillo estaba sano cuando de repente se volvió catatónico en unos pocos días, además de ser relativamente joven. Durante el transcurso de unas pocas semanas, cinco personas más fueron ingresadas en hospitales de la zona de la Bahía con el mismo aspecto de estar “congeladas” en una postura. ¿Cómo es que seis jóvenes sanos de repente habían desarrollado Parkinson severo? ¿Qué tenían todos ellos en común? El Dr. Langston no sabía que resolver este misterio transformaría nuestra forma de entender los mecanismos moleculares de la enfermedad de Parkinson.

Ejemplo de catatonia
Resultó que los seis consumían heroína. Es más, todos habían conseguido la droga de la misma fuente. El Dr. Langston consiguió una muestra para enviarla a analizar, lo que reveló que los “adictos congelados” no se habían inyectado heroína como ellos creían, sino un opiáceo sintético llamado MPPP (análogo del demerol, un analgésico opiáceo) junto a otro componente que no pudieron identificar. Sin embargo, MPPP no debería haber causado Parkinson. A pesar de que nunca se comercializó, en 1947 Albert Zeiring y John Lee sintetizaron y probaron MPPP en ratas, demostrando que dicho compuesto era relativamente seguro [1]. Por tanto, el componente sin identificar parecía ser el culpable, pero como no se sabía qué era, fue imposible analizar sus efectos.
Fue por aquel entonces cuando un amigo del Dr. Langston se topó con un caso de gran similitud en la literatura científica. En 1976, un estudiando de química llamado Barry Kidston desarrolló Parkinson repentinamente. Al igual que los seis pacientes del Dr. Langston, Kidston consumía opiáceos, pero al contrario que ellos era un aspirante a químico. Había leído el artículo original de 1947 de Ziering y Lee y decidió sintetizar su propio MPPP, puesto que era un opiáceo totalmente legal. Y lo consiguió. Fue capaz de sintetizar y usar durante varios meses su propio MPPP, hasta que un día llevó a cabo el proceso con prisa acelerando las reacciones. Al inyectarse el producto de la reacción final, se volvió catatónico. Los investigadores analizaron los residuos en el laboratorio y encontraron MPPP tal y como esperaban, pero también otro compuesto: MPTP. Esta impureza de MPTP se había formado porque Kidston sobrecalentó la mezcla durante su síntesis [2].
Cuando el Dr. Langston leyó dicho informe, supo que había dado con algo, ya que entonces pudo identificar la previamente desconocida sustancia como MPTP. Así que, en ambos incidentes, usuarios de opiáceos se habían inyectado MPTP y rápidamente desarrollado Parkinson, sugiriendo fuertemente que esta era la causa. Pero el Dr. Langston no fue el primero en pensarlo. Los investigadores que originalmente se encargaron del caso de Kidston habían administrado MPTP a ratas, las cuales se mostraron relativamente inafectadas [2]. Aun así, la evidencia circunstancial era fuerte y es sabido que las drogas en ocasiones afectan diferentes especies de forma distinta, así que el Dr. Langston decidió administrar MPTP a monos. Pocos días después de inyectarles MPTP, los monos desarrollaron síntomas parecidos al Parkinson [3]. Finalmente el Dr. Langston había encontrado al culpable, y más tarde escribiría un libro sobre su experiencia titulado: El caso de los adictos congelados.
Pero, ¿por qué y cómo causa Parkinson el MPTP? Resulta que el MPTP por sí solo es bastante inocuo, pero el cuerpo lo transforma en una potente neurotoxina llamada MPP+. El MPP+ mata las células uniéndose y afectando a las mitocondrias. Si recuerdas algo de la biología de la escuela (cosa que espero) las mitocondrias son la fuente de energía de la célula. Cuando el MPP+ se une a la mitocondria, le impide proveer dicha energía a la célula y las hace producir unas moléculas dañinas llamadas radicales libres. Estos cambios llevan a la muerte celular [4].
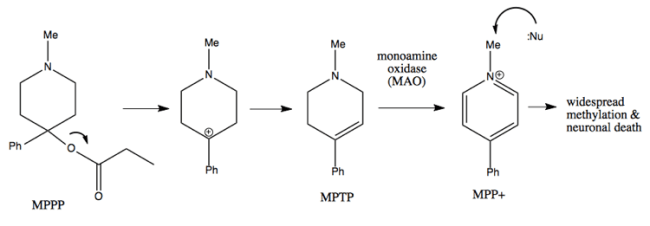
Si la reacción se calienta durante la síntesis del MPPP, se forma MPTP. En el cerebro, la enzima monoamina oxidasa transforma el MPTP en la neurotoxina MPP+.
Así que el MPP+ hace que las células se mueran, pero ¿por qué esta muerte celular provoca Parkinson? Primero vamos a empezar con algo de base sobre el Parkinson. A pesar de que la dopamina es mayormente conocida como el “compuesto de la recompensa” del cerebro, también juega un papel crucial en el control motor. Muchas de las neuronas dopaminérgicas del cerebro se encuentran en la substantia nigra, una región cerebral igualmente importante para la iniciación y el control del movimiento. El Parkinson se caracteriza por la muerte masiva y progresiva de las neuronas dopaminérgicas de la substantia nigra. Esta muerte celular en la substantia nigra es la que causa los síntomas motores del Parkinson.
Los análisis post-mortem del cerebro de Barry Kidston (el cual murió meses después de desarrollar Parkinson debido a una sobredosis) revelaron que el MPP+ causó la muerte de las neuronas dopaminérgicas de la substantia nigra de una forma muy similar indicando que el MPP+, de alguna forma, destruía estas neuronas de forma selectiva. Una cosa que distingue a las neuronas dopaminérgicas de los otros tipos de neuronas es que poseen el transportador de dopamina, DAT, el cual recicla la dopamina desde la sinapsis al interior de la célula de nuevo, de forma que la neurona puede reutilizarla. Desafortunadamente, el MPP+ tiene una estructura química similar a la dopamina de forma que DAT también transporta MPP+ al interior de la célula. Por eso el MPP+ solo entra en las neuronas dopaminérgicas, y solo estas neuronas mueren, dando lugar a una muerte celular selectiva de las neuronas dopaminérgicas de las substantia nigra, tal y como ocurre en la enfermedad de Parkinson.

El MPP+ y la dopamina son transportados por el transportador de dopamina (DAT) al interior de la neurona. Una vez ahí, el MPP+ altera la cadena de transporte de electrones de las mitocondrias, impidiéndoles proveer energía a la célula. El MPP+ también altera la función de varias enzimas.
Aunque las circunstancias de los “adictos congelados” fueron innegablemente trágicas, existe un aspecto positivo. Para los pacientes, todos respondieron a la típica medicación para el Parkinson. De hecho, varios de ellos – incluyendo el paciente original, George Carrillo – se sometieron a un asombroso tratamiento: el trasplante de neuronas dopaminérgicas fetales en el cerebro. Un reciente seguimiento ha demostrado que estos trasplantes son seguros e increíblemente efectivos a la hora de reducir algunos de los síntomas del Parkinson [5].
A mayor escala, el MPTP revolucionó la investigación del Parkinson. Aunque actualmente desconocemos las causas que llevan a la muerte de las neuronas dopaminérgicas en Parkinson (visita el post en NeuWrite de Caley Bromer sobre los pesticidas como posible causa), el MPTP permite a los investigadores modelar algunos aspectos claves de la patología detrás del Parkinson. A pesar de que existían otros modelos anteriores al MPTP, éste replica mucho mejor (aunque todavía de forma imperfecta) la patología y los síntomas de comportamiento del Parkinson. De hecho, algunos investigadores han desarrollado procedimientos en los que combinan dosis crónicas de MPTP con otras drogas para replicar la naturaleza progresiva del Parkinson [6]. No solo ha ayudado a comprender el Parkinson, sino que dichos modelos también permiten a los investigadores a desarrollar y probar nuevos tratamientos, pensados para reducir los síntomas del Parkinson o incluso prevenir la muerte de las neuronas.

Cinco de los “adictos congelados”.
Cuando le pidieron ayuda al Dr. Langston para diagnosticar al primer paciente de MPTP, no se imaginaba las asombrosas consecuencias que su investigación traería para el estudio de la enfermedad de Parkinson. Es increíble pensar en el potencial de estos pequeños eventos aleatorios para cambiar el mundo de tal manera. Si los efectos neurotóxicos del MPTP no se hubieran descubierto nunca, es posible que los investigadores aun estuvieran intentando encontrar un modelo de Parkinson. Pero gracias a todo esto, ahora tienen una forma de investigar la naturaleza del Parkinson y a la vez de desarrollar y probar nuevos tratamientos orientados a mejorar la vida de los millones de personas afectadas con esta enfermedad en todo el mundo.
Referencias
- Ziering, A.; Lee, J. (1947). “Piperidine derivatives; 1,3-dialkyl-4-aryl-4-acyloxypiperidines”.The Journal of Organic Chemistry. 12 (6): 911–914. doi:1021/jo01170a024.PMID18919744.
- Davis, G. C., Williams, A. C., Markey, S. P., Ebert, M. H., Caine, E. D., Reichert, C. M., & Kopin, I. J. (1979). Chronic Parkinsonism secondary to intravenous injection of meperidine analogues. Psychiatry Research, 1(3), 249–254.
- Langston, J. W., Forno, L. S., Rebert, C. S., & Irwin, I. (1984). Selective nigral toxicity after systemic administration of 1-methyl-4-phenyl-1,2,5,6-tetrahydropyrine (MPTP) in the squirrel monkey. Brain Research, 292(2), 390–394.
- Dauer, W., & Przedborski, S. (2003). Parkinson’s Disease: Mechanisms and Models. Neuron, 39(6), 889–909. http://doi.org/10.1016/S0896-6273(03)00568-3
- Hallett, P. J., Cooper, O., Sadi, D., Robertson, H., Mendez, I., & Isacson, O. (2014). Long-Term Health of Dopaminergic Neuron Transplants in Parkinson’s Disease Patients. Cell Reports, 7(6), 1755–1761. http://doi.org/10.1016/j.celrep.2014.05.027
- Meredith, G. E., & Rademacher, D. J. (2011). MPTP Mouse Models of Parkinson’s Disease: An Update. Journal of Parkinson’s Disease, 1(1), 19–33. http://doi.org/10.3233/JPD-2011-11023
Imágenes
Imagen de portada: http://d.gr-assets.com/books/1388804488l/1510265.jpg. Tomada de: Langston, J. W.; Palfreman, J. (May 1995). The Case of the Frozen Addicts. Pantheon Books. ISBN 0-679-42465-2.
Imagen 1: http://www.minddisorders.com/images/gemd_01_img0029.jpg
Imagen 2: Adaptada de [4]: http://doi.org/10.1016/S0896-6273(03)00568-3
Imagen 3: http://www.cureffi.org/2015/03/04/organic-chemistry-14/
Imagen 4: https://mmcneuro.files.wordpress.com/2013/12/frozen.jpg?w=315&h=266

You must be logged in to post a comment.