
¿Se puede heredar el trauma familiar?
La epigenética tras el “trauma generacional”
Artículo original de Nicole Mlynaryk.
Traducción de Elena Blanco-Suarez.
La moda de 23 and Me acaba de llegar oficialmente a mi familia. Mis padres nacieron en Polonia, así que los resultados no han sido muy sorprendentes, pero se han generado nuevas preguntas al ver las generaciones de historia familiar que han surgido de una muestra de escupitajo. Cuando mis hermanas y yo nos sentamos a la mesa con mis padres y un poco de tiempo libre, decidimos preguntar sobre nuestro árbol genealógico. Empezamos con los nombres y lugares que ya conocemos, pero el árbol creció rápidamente, y con cada nueva rama iban saliendo nuevos personajes e historias que eran difíciles de creer. Tomamos nota. Me enteré de la existencia de grandes familias en pequeñas granjas. Adolescentes que fueron enviados en barcos a tierras extranjeras para encontrar trabajo y mandar dinero a casa. Padres que perdieron a sus hijos; hijos que perdieron a sus padres. Cada vida personalmente afectada por las dos guerras mundiales. Y había también una deportación a Siberia. Me fui pensando no solo sobre mi familia, sino también en como todas las familias acarrean esas historias tan increíbles de supervivencia, a través de dificultades que muchos de nosotros ni siquiera experimentaremos nunca. Y aun así, cada vez hay más evidencias sobre la idea de trauma generacional que sugiere que las generaciones más recientes no se han librado de las consecuencias.
En el eterno debate de herencia versus crianza, confiamos en el hecho de que nuestras experiencias vitales no tienen efecto en nuestro código genético. Nuestro comportamiento y estado de salud están claramente definidos por nuestro estilo de vida, pero estos aspectos solo pueden pasarse a nuestros hijos a traces de medios sociales y culturales. O al menos eso creíamos. Una nueva forma de herencia transgeneracional acaba de salir a la luz, en la cual los efectos del trauma y el estrés en la vida de un progenitor podrían llegar a pasarse a sus hijos en formas que definirían su salud física, cognitiva y su comportamiento. Muchos estudios ya han utilizado esta idea para explicar los problemas de salud observados en la descendencia de supervivientes del Holocausto, refugiados, veteranos, y aquellos que han sufrido pobreza, racismo, o desastres naturales [1-4]. ¿Pero cómo es eso posible?
A pesar de que tus experiencias vitales no afectan tu código genético (esas en las que los resultados de 23 and Se me basan), sí que afectan tu epigenética. Alrededor de tu ADN existe un complicado sistema de herramientas moleculares que deciden que genes se activan y cuáles no, cuando y donde. Si tus genes son la lista de ingredientes en una receta, la epigenética son las instrucciones de qué hacer con ellos. Y el sistema responde a cambio en el ambiente, es decir, cuando un evento traumático tiene lugar, tu cuerpo reacciones y escribe instrucciones nuevas. Lo que no sabíamos era que esas instrucciones pueden pasarse a la descendencia. Esas herramientas epigenéticas juegan un papel muy importante en dirigir el desarrollo embrionario, y pequeños cambios en dichas instrucciones pueden llevar a desencadenar una cascada de eventos moleculares que dictaran la función del cerebro, el cuerpo y el comportamiento.
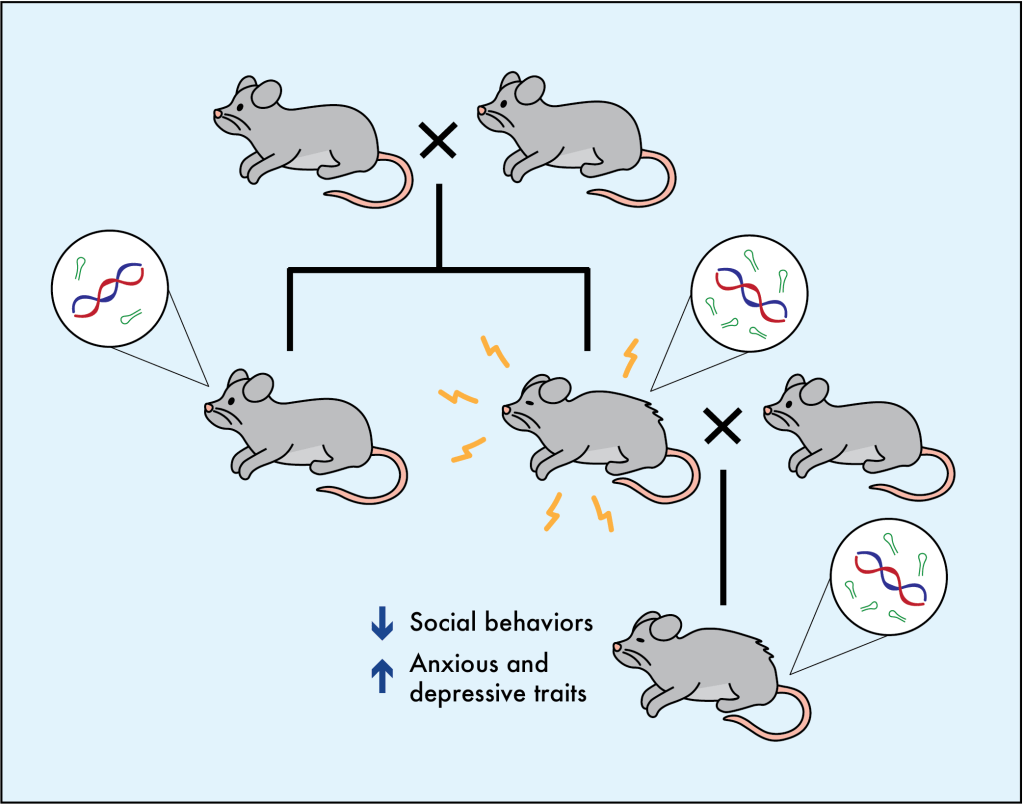
Esto tiene grandes implicaciones. Pero muchos científicos se muestran escépticos de los estudios en humanos, especialmente por la dificultad que conlleva separar que aspectos con transmitidos epigenéticamente versus aquellos que son resultado de la dinámica social derivada del trauma. Datos más fiables proceden de los estudios con ratones, donde estos aspectos pueden controlarse de manera más precisa. En estos experimentos los ratones se someten a eventos estresantes (por ejemplo un shock dolorosa, separación de los progenitores, etc…) lo cual induce un cambio epigenético que puede medirse [5-7]. Por ejemplo, el esperma de ratones macho expuestos a estrés sufre cambios repentinos en los niveles de unas moléculas epigenéticas llamadas microRNAs, las cuales funcionan bloqueando la expresión de ciertos genes. Lo que es interesante es que la descendencia de dichos ratones se comporta de manera diferente cuando se compara con otros ratones, mostrando características de ansiedad y depresión, menor sociabilidad, y con comportamientos más temerario. Lo que es más, la descendencia macho de los ratones estresados muestran las mismas alteraciones epigenéticas en su esperma (más o menos microRNA), incluso cuando no han experimentado ellos mismos el evento traumático. Lo que es importante destacar es que los ratones que no han crecido con sus padres, lo que indica que estos cambios no ocurren a través de interacciones sociales con progenitores estresados. Dando un paso más allá para probar que estos comportamientos son debidos a cambios epigenéticos, los científicos inyectaron microRNAs directamente en los embriones y ver el mismo cambio en comportamiento en aquellos animales y su descendencia, incluso cuando el evento traumático no ocurrió. Uno de los estudios pudo demostrar que estos cambios epigenéticos llevan a una reprogramación genética del hipotálamo, una región cerebral implicada en regular las respuestas a estrés [7].
¿Podemos extrapolar estos experimentos en ratones a nosotros? En un estudio especialmente interesante, un grupo observó estos microRNA en ratones y hombres. Los hombres adultos completaron el test sobre Experiencias Adversas de la Infancia (ACE en sus siglas en ingles), el cual pregunta sobre varias formas de abuso o negligencia experimentadas durante la infancia de una persona. Una puntuación alta en el ACE se correlaciona fuertemente con comportamientos asociados a estrés y problemas de salud en ese individuo y sus hijos. Los investigadores compararon el perfil epigenético del esperma de los hombres con el de los ratones estresados. Sorprendentemente, encontraron los mismos cambios en el microRNA en los hombres y en los ratones, y cuanto más alta era la puntuación del test ACE, mayor era la probabilidad de encontrar coincidencias con el perfil epigenético de los ratones estresados [8].
¿Qué podemos hacer? Los efectos en el comportamiento derivados de estrés traumático pueden transmitirse hasta cuatro generaciones [9] – ¿pero podemos parar ese ciclo? Algunos estudios sugieren que potencialmente se pueden revertir los cambios epigenéticos, incluyendo buena salud materna y buena nutrición durante el embarazo. Aunque aún tenemos mucho que aprender sobre la epigenética y como da forma a nuestra función cerebral, una mejor comprensión podría ayudarnos a desarrollar herramientas biológicas que reprogramasen selectivamente el sistema. Pero hasta que podamos directamente modificar a nivel molecular, al menos podemos intentar mitigar los efectos del trauma generacional. California ha nombrado recientemente a la Doctora Nadine Burke Harris primera Cirujana General del estado, y está trabajando para incorporar el test ACE de trauma infantil en las visitas estándar al doctor, tanto para niños como para sus padres. Esto se hace sabiendo que una intervención temprana con el apoyo médico, y psicológico, y ambientes positivos se pueden mejorar significativamente los resultados en la salud. Conocer el trauma en la historia familiar propia puede ser crítico (no se puede solucionar lo que desconoces). Y si nuestra epigenética es capaz de responder de forma flexible a las circunstancias, quizás tratar el trauma sería suficiente para alcanzar el nivel molecular. Pero quizás lo más efectivo e importante sería el promover una mejor concienciación de los daños a largo plazo que un trauma puede causar ayudándonos así a prevenirlo de la mejor manera posible.
Referencias
- Yehuda R, Daskalakis NP, Bierer LM, et al. (2016) Holocaust Exposure Induced Intergenerational Effects on FKBP5 Methylation. Biological Psychiatry, 80:372–380.
- Costa DL, Yetter N, DeSomer H. (2018) Intergenerational transmission of paternal trauma among US Civil War ex-POWs. PNAS, 115(44): 11215–11220.
- Vågerö D, Pinger PR, Aronsson V, van den Berg GJ. (2018) Paternal grandfather’s access to food predicts all-cause and cancer mortality in grandsons. Nature Communications, 9: 5124.
- Aroke EN, Joseph PV, Roy A, Overstreet DS, et al. (2019) Could epigenetics help explain racial disparities in chronic pain? Journal of Pain Research, 12: 701–710.
- Dias BG and Ressler KJ. (2014) Parental olfactory experience influences behavior and neural structure in subsequent generations. Nature Neuroscience, 17(1): 89–96.
- Gapp K, Jawaid A, Sarkies P, et al. (2014) Implication of sperm RNAs in transgenerational inheritance of the effects of early trauma in mice. Nature Neuroscience, 17(5): 667–669.
- Rodgers AB, Morgan CP, Adrian Leu N, Bale TL (2015) Transgenerational epigenetic programming via sperm microRNA recapitulates effects of paternal stress. PNAS, 112(44): 13699–13704.
- Dickson DA, Paulus JK, Mensah V, et al. (2018) Reduced levels of miRNAs 449 and 34 in sperm of mice and men exposed to early life stress. Translational Psychiatry, 8: 101.
- van Steenwyk G, Roszkowski M, Manuella F, et al. (2018) Transgenerational inheritance of behavioral and metabolic effects of paternal exposure to traumatic stress in early postnatal life: evidence in the 4th generation. Environmental Epigenetics, 4(2).
Imagen principal de Marco Verch.
Licencia: https://creativecommons.org/licenses/by/2.0/

You must be logged in to post a comment.